El 20 de febrero de 2023, la Comisión Europea autorizó la comercialización de tremelimumab. Este fármaco, combinado con durvalumab, tiene indicación en primera línea en el carcinoma hepatocelular avanzado o irresecable (estadio B y C de la BCLC). El informe público europeo de evaluación (EPAR, por sus siglas en inglés) está basado en el ensayo HIMALAYA. Al revisar la eficacia en ese ensayo, destacamos un aspecto que puede ser clave para el posicionamiento.
- El brazo comparador es sorafenib. Actualmente la terapia que ha obtenido mejores resultados en términos de eficacia es atezolizumab + bevacizumab, tratamiento preferente financiado (ver IPT). Por lo tanto, lo interesante sería comparar tremelimumab + durvalumab frente atezolizumab + bevacizumab.
- Encontramos un metaanálisis (Fulgenzi et al, 2022) que combina 9 ensayos clínicos de fármacos en hepatocarcinoma. Entre ellos se encuentran el IMbrave150 (atezolizumab + bevacizumab frente a sorafenib) y el HIMALAYA (tremelimumab + durvalumab frente a sorafenib). La comparación indirecta de supervivencia global (SG) da como resultado un HR (hazard ratio) 0,74 (IC del 95 % 0,52-1,06) para la combinación de atezolizumab vs. la de tremelimumab. Por tanto, no se obtienen diferencias significativas entre ambas terapias. Sin embargo, se utilizaron datos inmaduros del ensayo IMbrave (mediana de seguimiento de 6,8 meses).
- A diferencia del metaanálisis, para una comparación indirecta propia utilizamos los datos actualizados del ensayo IMbrave (mediana de seguimiento de 15,6 meses). De esta forma se obtiene un HR 0,85 (IC del 95% 0,63 – 1,14). De nuevo, la comparación carece de diferencia estadísticamente significativa (ver tabla).
- En el ensayo pivotal, el tiempo hasta el deterioro de la calidad de vida global mejoró significativamente con tremelimumab+ durvalumab frente a sorafenib HR 0,76 (IC del 95 %: 0,61-0,96). Esto también ocurrió con atezolizumab + bevacizumab frente a sorafenib HR 0,63 (IC del 95% CI, 0,46 a 0,85).
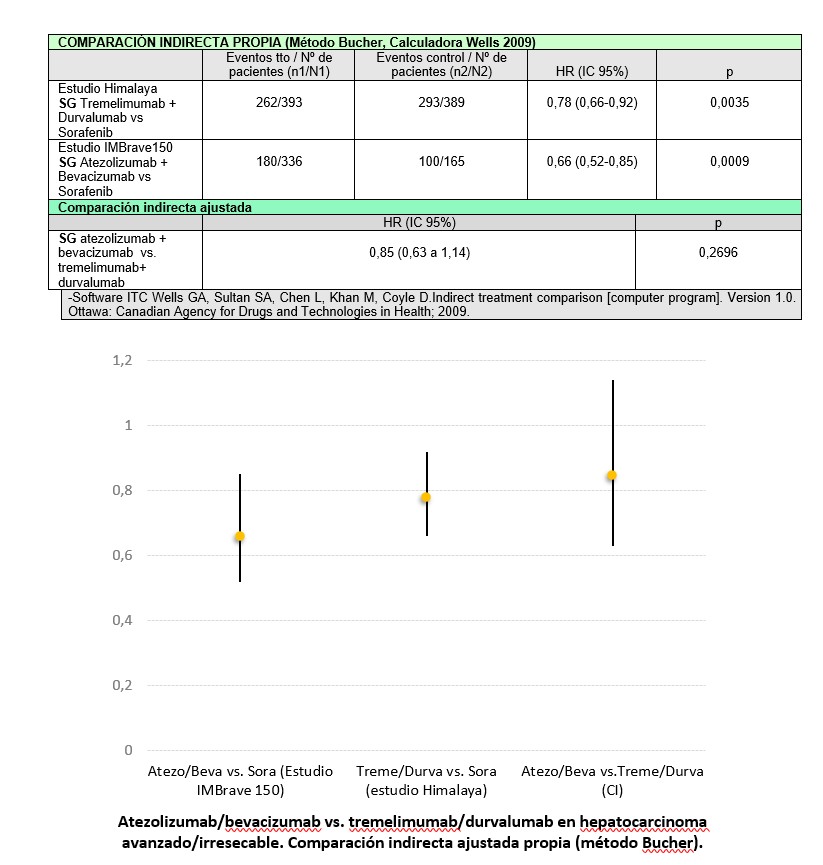
Por tanto, en términos de eficacia, la combinación de tremelimumab + durvalumab no ha demostrado beneficio clínico frente a atezolizumab + bevacizumab, el estándar actual.
NOTA: este es un avance de un informe en desarrollo que será publicado en los próximos meses en la web de GENESIS-SEFH, el cual contará con información más completa y detallada.
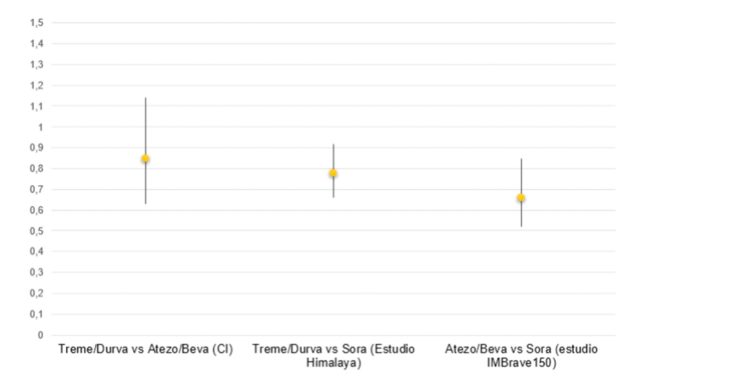
Fe de erratas: Esta entrada fue publicada el 07/08/2023. El gráfico se ha modificado por una errata en el orden del título de la comparación indirecta «tremelimumab+durvalumab vs. atezolizumab+bevacizumab» se sustituye por «atezolizumab+bevacizumab vs. tremelimumab+durvalumab», fecha de modificación 25/09/2023.










One Comment
Pingback: Lo que perdemos sin REvalMed – Centro de Información de Medicamentos